|

在制药行业的GMP洁净室管理中,空气颗粒监测扮演着至关重要的角色,主要分为两大类别:洁净室分级与日常环境监测。尽管两者均为确保药品生产环境质量的关键环节,但许多从业者对它们的异同点认识模糊。
对于GMP洁净室的日常环境监测,其规划通常由洁净室负责人依据实际情况定制。然而,缺乏明确指导往往导致两种极端情况:一是监测流程过于繁琐,增加了对关键区域的干扰及潜在污染风险;二是简单地照搬洁净室分级标准制定监测计划,忽视了基于药品污染威胁的风险评估。实际上,日常环境监测应聚焦于识别并应对药品在洁净室内可能暴露的高风险区域,因此其取样点与分级时的取样点可能大相径庭。 接下来,我们深入探讨GMP洁净室分级与日常环境监测的异同及注意事项,并介绍专注于洁净室颗粒监测的北京中邦兴业公司能提供的支持。 洁净室分级的核心 洁净室分级主要聚焦于洁净室自身的性能评估。这一过程遵循ISO 14644-1:2015标准,在不额外增设取样点的情况下,全面考量洁净室的空气质量。分级结果反映了洁净室作为一个整体的性能水平,要求所有取样点的空气颗粒浓度均需符合预设等级。分级测试通常每半年至一年进行一次,因此其数据统计的有效性相对有限。简而言之,洁净室分级旨在验证洁净室的空气质量是否优于GMP规定的等级限值,确保生产环境的基本质量水平。
值得注意的是,无论是洁净室分级还是日常环境监测,关键在于理解并应用各自的核心原则,避免将两者混为一谈。北京中邦兴业公司,作为洁净室颗粒监测领域的专家,能够提供专业的咨询、测试方案定制及数据分析服务,帮助制药企业精准把握洁净室空气质量状况,优化监测流程,确保药品生产环境的安全与合规。 在EU GMP附录1 无菌药品、FDACGMP及我国GMP中都规定了洁净室分级应按照ISO 14644-1:2015中定义的方法进行,但不同的是,EUGMP和我国GMP附录1中有其自身的颗粒限值要求,包括了A级区进行分级和日常监测的5um颗粒限值,但在ISO 14644-1:2015中,等同于A级区的Class5并未规定5um颗粒的任何限值。 01 ISO 14644-1:2015关于洁净室分级内容摘要 使用查找表定义洁净室分级所需的取样点数量 规定取样点应均匀分布在洁净室中 要求采样探针的位置应与洁净室该区域的工作活动处于同一高度 在提供单向流的情况下,应使用等动力探头,且探头应朝向气流源 规定了每个取样点采集的最小取样量 如果在一个取样点发生多次取样,则该取样点的结果应取平均值 如果所有取样点的尘埃粒子浓度低于洁净室等级要求的最大允许空气颗粒浓度,则认为该洁净室已通过分级 何为洁净室日常环境监测? 洁净室日常环境监测是一种基于风险评估的定期监测活动,旨在确保药品生产环境在持续运营中维持既定的清洁标准。与洁净室分级不同,日常环境监测更加灵活且针对性强,它依据生产过程中的污染风险等级,对不同区域实施不同频率的监测。
在日常环境监测中,关键区域(如直接接触药品的区域、高风险操作区等)可能需要每天进行监测,以确保其空气质量始终符合GMP要求。而对于次要关键区域,监测频率可适当降低,如每周进行一次。这种高频次的监测不仅提供了丰富的数据支持,还使得企业能够对洁净室的污染水平进行趋势分析,及时发现并纠正潜在问题。
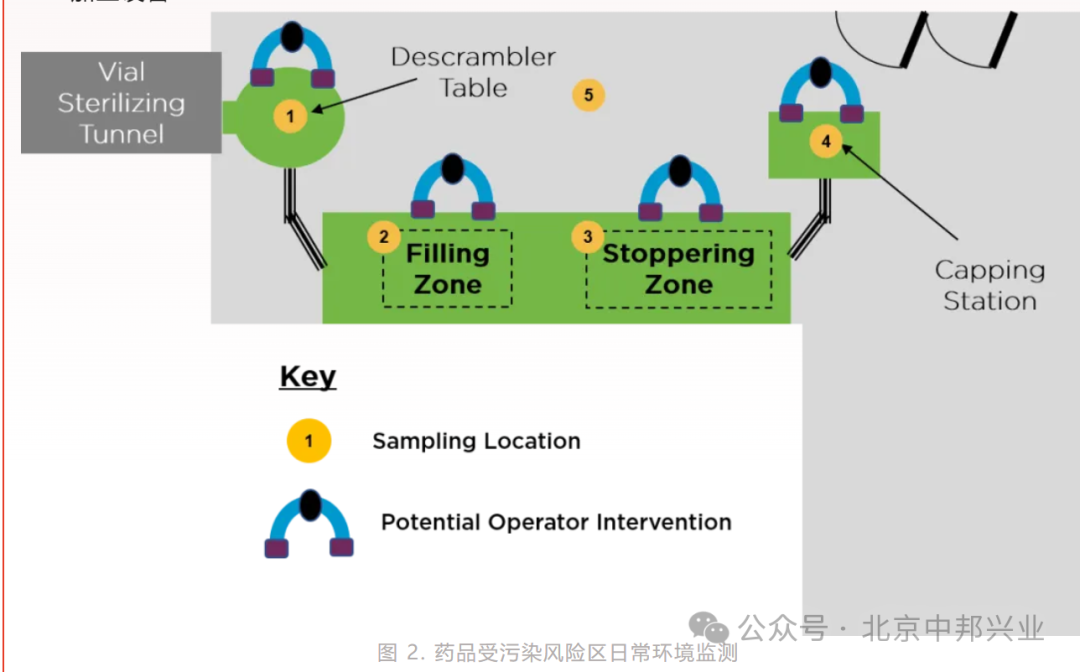
取样点的选择在日常环境监测中尤为重要。与洁净室分级中规定的最少取样点数量不同,日常环境监测的取样点是根据具体生产过程的风险评估结果来确定的。这意味着,取样点应设置在那些可能使药品面临更高污染风险的位置,如物料入口、人员通道、设备周围等。通过这种方式,日常环境监测能够更准确地反映药品生产过程中实际面临的污染威胁,并证明这些关键区域在药品生产前及生产中的正常运行状态。 综上所述,洁净室日常环境监测是一种高度定制化、风险导向的监测策略,它通过对关键区域的高频次监测和基于风险评估的取样点选择,确保了药品生产环境在持续运营中的清洁度和安全性。 02 可能使药品面临污染风险的位置包括但不限于 可能存在操作员干预的位置 菌制造和灌装区 灭菌设备包装 药物配置区 加工设备
GMP关于洁净室空气颗粒计数的相关摘要 根据风险评估和洁净室分级的情况,洁净室和空气净化设备需在运行时进行日常监测。 使用自动化系统进行监测的取样量通常是所用系统取样率的函数,取样量不必与洁净室分级时所用取样量相同。 A级区应以适当的频率和适当的取样量进行监测,以便在超过警报限时发现所有人为干预、偶发事件和任何系统的损坏。
在A级和B级区,≥5.0μm颗粒浓度计数的监测具有特殊意义,因为它是及时发现问题的重要诊断工具。由于电子噪声、杂散光、重合等原因,5.0μm颗粒计数可能是错误计数,但是,连续或定期的低水平计数是可能发生污染事件的指示器,应进行调查。 激光尘埃粒子计数器主要优势功能 Lighthouse ApexZ3/50便携式空气颗粒计数器,有助于确保分级和日常监测都遵循标准设定的SOP(标准操作程序)。
定制化SOP测试程序: 交互式SOP测试程序,可以统一设定粒径、行动限、警报限等,实现仪器组间共享SOP测试程序和测试结果。 点位存储功能: 用户可以在设备中预先存储多达2500个不同的监测点位信息。这些点位信息包括但不限于位置名称、监测参数等。被存储过的信息,用户在后续监测过程中就可以直接使用,无需每次手动输入位置名称,提高监测效率。
高效的数据管理功能: 电子签名:测试完成后,主管可通过web浏览器远程复核和审批。一旦通过审批,电子签名将附在最终报告上,并可以安全的电子格式导出。 数据库安全且加密,普通用户无权删除记录,确保数据的完整性和安全性。 21 CFR Part 11合规性:提供微软活动目录控制的多级登录和电子签名的用户名和密码,符合法规要求。 GMP等级审计追踪功能:内置筛选功能,可快速找到审核过程所需的数据并出具报告。 来源:北京中邦兴业
版权声明:
本站部分内容、观点、图片、文字、视频来自网络,仅供大家学习和交流,真实性、完整性、及时性本站不作任何保证或承诺。如果本站有涉及侵犯您的版权、著作权、肖像权的内容,请联系我们(021-62511200),我们会立即审核并处理。
|
|||||||||||